Mathématiquement
On identifie l'étage d'oxydation des atomes qui n'en ont qu'un.
L'hydrogène
Son étage d'oxydation vaut toujours +1 sauf dans :
- H2 où il est égal à zéro
- les hydrures métalliques (ex : NaH) où il vaut -1
L'oxygène
Son étage d'oxydation vaut toujours -2 sauf dans :
- O2 où il est égal à zéro
- H2O2 où il vaut -1
Certains métaux
Certains métaux ne possèdent qu'un étage d'oxydation :
- les alcalins (famille Ia) : EO = +1
- les alcalino-terreux (Famille IIa) : EO = +2
- les terreux (Famille IIIa) : EO = +3
- Ag : EO = +1
- Zn : EO = +2
On identifie la charge globale de l'édifice moléculaire.
molécule
Par définition, une molécule est neutre. Elle ne possède aucune charge, la somme de tous les étages d'oxydation des atomes devra donc valoir zéro.
ion
Par définition, un ion est chargé. La somme de tous les étages d'oxydation des atomes devra donc être égale à la charge de l'ion.
On calcule l'étage d'oxydation manquant (on utilise une inconnue).
Exemple Na2Cr2O7
- Na est un alcalin : EO= +1
- Cr : EO inonnue, à déterminer
- O : EO = -2
C'est une molécule, la somme sera donc égale à zéro :
2 (+1) + 2x + 7 (-2) = 0
2x +2 - 14 = 0
2x = 12
x= 6 (EO du chrome = +6)
Exemple SO4--
- S : EO inconnue, à déterminer
- O : EO = -2
Il s'agit d'un ion dont la charge vaut -2. La somme des EO sera donc égale à -2
x + 4 (-2) = -2
x = -2 +8 = 6 (EO du S =+6)
Par dessin
Cette méthode nécessite de pouvoir dessiner la molécule. Une fois le dessin réalisé, on va analyser pour chaque liaison le nombre d'électrons que chaque atome gagne ou perd (en fonction des électronégativités).
- Lorsqu'un atome est plus électronégatif qu'un autre, il attire à lui les électrons, il gagne donc une charge -1 (on ajoute -1 à l'EO de l'atome)
- Lorsqu'un atome est moin électronégatif, c'est le contraire, on ajoutera +1 à l'EO)
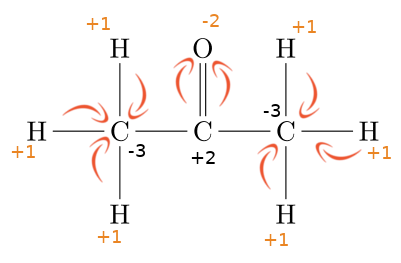
Dans cet exemple, nous utilisons les électronégativités pour attribuer les charges aux atomes :
- 2,2 pour H
- 2,5 pour C
- 3,5 pour O
Les H étant moins électronégatifs que les C, chacun verra son électron partagé s'éloigner en donnant une charge +1 à chaque H. Le C gagnera une charge négative à chaque fois.
Pour l'oxygène, étant plus électronégatif que le carbone, il attirera à lui les électrons mis en partage par le carbone. L'O gagnera des charges négatives (1 par liaison) pendant que le carbone gagnera des charges +.
Entre les atomes de carbone, il n'y a pas de déplacements d'électrons.







