Apprendre
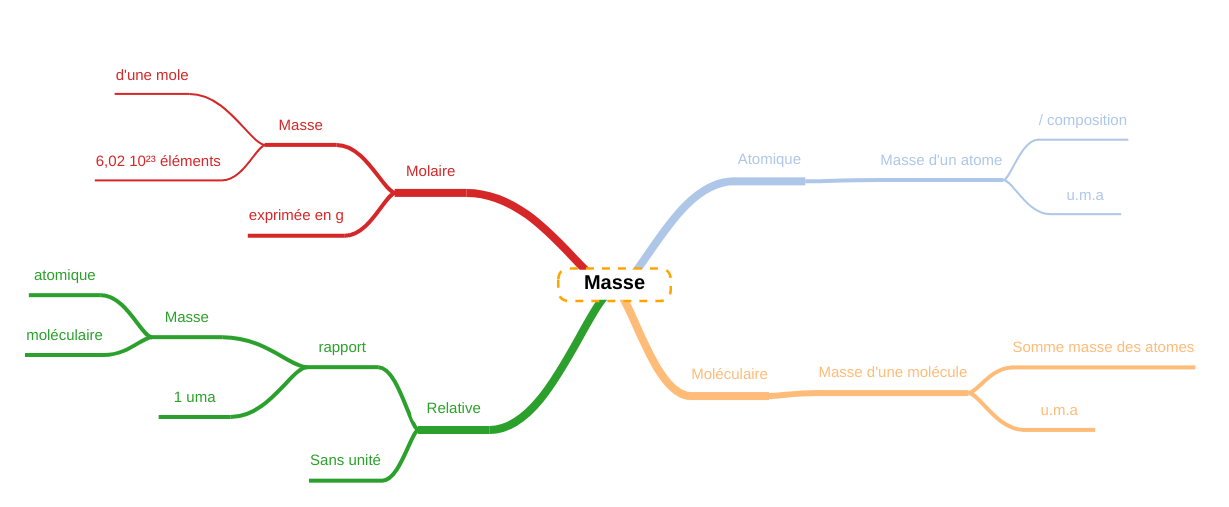
Masse atomique relative
L'élement carbone possède 3 isotopes : le carbone 12, le carbone 13 et le carbone 14. Comme ce sont tous des nucléides du carbone, ils ont tous : Leur différence de masse provient de leur composition différente en neutrons, respectivement 6, 7 et 8. Dans le tableau périodique, ils sont tous les 3 rassemblés en une seule case, appelée "carbone", c'est l'élément. La masse attribuée à cet élément est appelée masse atomique. Pourquoi fonctionner ainsi ? Simplement parce que si je prend x grammes d'un élément, je vais très certainement retrouver les différents isotopes qui existent dans la nature en quantité globalement similaire à leur abondance. Cette valeur représente la masse atomique. Elle est exprimée en Unité de Masse Atomique (U.M.A). L'U.M.A représente le douzième de la masse du nucléide 12C. Pour qu'elle soit RELATIVE il faut la diviser par 1 U.M.A de telle façon à ce que la masse atomique relative n'ait pas d'unités ! Cette formule permet aussi de calculer les paramètres isotopiques, si on connait la masse atomique relative. C'est une variante d'exerice. En vous fournissant la masse atomique relative et toutes les informations sur les isotopes sauf une, vous pouvez facilement retrouver la donnée manquante.





3 nucléides
1 élément
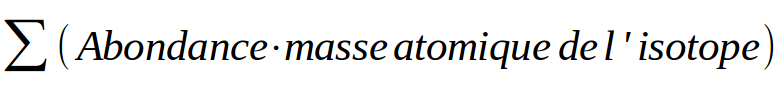

Masse moléculaire relative
Ainsi calculer la masse d'une molécule c'est faire des additions et des multiplications. Nous obtenons un chiffre exprimé en u.m.a ; la masse moléculaire. La masse moléculaire relative est ce même nombre, divisé par 1 uma, soit, sans unité. La masse molaire est toujours ce même nombre accompagné de l'unité (g/mol). Elle représente la masse d'une mole (6,02 1023 molécules) de ce corps. N'oublions pas les cristaux ! Actuellement, nous avons considéré les molécules toutes seules. Nous avons considéré que ces matières parfois solides ne comportaient pas d'eau (anhydre). Ce n'est pas toujours le cas, il arrive bien souvent que nous ayons des substances cristallisées. Dans ce cas, un certain nombre de moécules d'eau sont présentes dans les cristaux, attachées aux molécules de ce corps. On fait alors suivre leur formule d'un point et du nombre de molécules d'eau attachées : Cr(NO3)3•9H2O Dès que l'on voit une telle structure, il faut ajouter à la masse de la molécule (le nitrate de chrome (III) dans notre exemple), la masse des molécules d'eau (on ajoutera ici 9x 18g/mol).
La masse d'une molécule, c'est (simplement) la somme des masses des atomes qui la composent